ベトナムへの医療機器の輸入は複雑なプロセスです, 現在の法規制への厳格な準拠が必要です. ヘルスケア分野で重要な役割を果たしています, 医療機器は厳しい品質基準を満たす必要がある, 安全かつ合法的. この記事では、医療機器を輸入するために必要な手順について詳しく説明します。, 書類作成から通関手続きまで, 企業が規制を理解し、効果的に施行できるよう支援する.
記事の内容
医療機器とは何ですか??
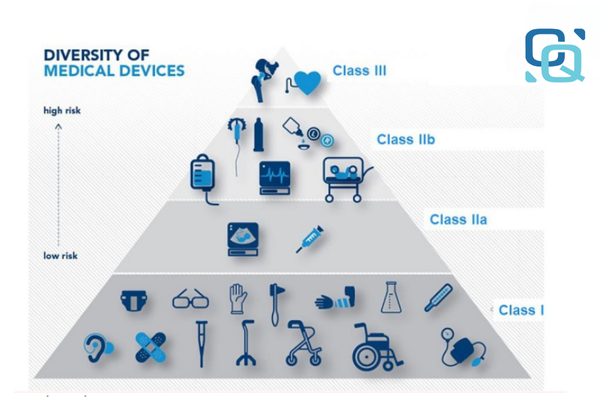
医療機器にはあらゆる種類の機械が含まれます, 道具, 医療分野で診断に使用される材料または製品, 処理, 病気を監視または予防する. 政令 36/2016/ND-CP および関連法的文書の規定による, 医療機器はリスクレベルに基づいて分類されます, 4つのグループが含まれます: a, B, CとD. そこに:
-
タイプA: デバイスのリスクは低レベルです, 医療用綿棒のようなもの, 医療テープ.
-
タイプB: 中リスクのデバイス, たとえば、血圧計.
-
タイプC: ハイリスク機器, X線検査装置のように.
-
タイプD: このデバイスは非常に危険です, 血液透析装置や埋め込み型装置など.
この分類は、輸入許可と品質検査の要件に直接影響します。.
医療機器の輸入に関する法的規制
ベトナムで, 医療機器の輸入は多くの国家機関の管理下にあります, 主に保健省, 税関総局および関連機関. この活動を規制する主な法的文書には次のものがあります。:
-
法令 36/2016/ND-CP: 医療機器管理規定, 輸入および流通の条件を含む.
-
政令 169/2018/ND-CP: 修正する, bổ sung một số quy định của Nghị định 36/2016/NĐ-CP.
-
Thông tư 30/2015/TT-BYT: Hướng dẫn về nhập khẩu thiết bị y tế.
-
Thông tư 14/2018/TT-BYT: Bổ sung quy định về phân loại và kiểm định thiết bị y tế.
Theo các quy định này, nhập khẩu thiết bị y tế phải có giấy phép lưu hành hoặc giấy phép nhập khẩu, trừ một số trường hợp đặc biệt được miễn. Doanh nghiệp cần nắm rõ các yêu cầu này để tránh vi phạm pháp luật.

医療機器を輸入する手順
Để nhập khẩu thiết bị y tế vào Việt Nam, 企業は次の手順を実行する必要があります:
1. 医療機器の種類を確認する
Trước khi nhập khẩu, doanh nghiệp cần xác định thiết bị thuộc nhóm nào (a, B, C hay D) dựa trên mức độ rủi ro. Điều này quyết định loại giấy phép cần xin và các yêu cầu kiểm định. 例えば:
-
Thiết bị loại A, B thường chỉ cần đăng ký lưu hành.
-
Thiết bị loại C, D yêu cầu giấy phép nhập khẩu và kiểm định chất lượng nghiêm ngặt hơn.
Doanh nghiệp có thể tham khảo danh mục phân loại thiết bị y tế do Bộ Y tế ban hành hoặc liên hệ đơn vị tư vấn để xác định chính xác.
2. 法的文書の準備
Hồ sơ nhập khẩu thiết bị y tế bao gồm nhiều tài liệu quan trọng, tùy thuộc vào loại thiết bị. Một bộ hồ sơ cơ bản thường bao gồm:
-
Giấy phép lưu hành: Đối với thiết bị loại A, B, doanh nghiệp cần đăng ký lưu hành tại Bộ Y tế. Đối với loại C, D, cần xin giấy phép nhập khẩu.
-
Giấy chứng nhận chất lượng (品質証明書): Do cơ quan có thẩm quyền tại nước xuất khẩu cấp, chứng minh thiết bị đạt tiêu chuẩn quốc tế (ISO 13485, CE, FDA…).
-
委任状 (Letter of Authorization): Từ nhà sản xuất hoặc nhà phân phối chính thức, ủy quyền cho doanh nghiệp nhập khẩu tại Việt Nam.
-
商業契約 (Commercial Contract): Ghi rõ thông tin về lô hàng, 量, giá trị và điều khoản giao hàng.
-
商業送り状 (商業送り状): Chi tiết giá trị hàng hóa.
-
パッケージ (包装内容明細書): Thông tin về số lượng, trọng lượng và cách đóng gói hàng hóa.
-
原産地証明書 (原産地証明書): Xác nhận nguồn gốc thiết bị, giúp hưởng ưu đãi thuế (ある場合).
-
Tài liệu kỹ thuật: Mô tả chi tiết về thiết bị, bao gồm thông số kỹ thuật, hướng dẫn sử dụng và bảo trì.
Các tài liệu này cần được dịch thuật công chứng sang tiếng Việt nếu là ngôn ngữ nước ngoài.
3. 輸入ライセンスを申請する
Đối với thiết bị y tế loại C và D, doanh nghiệp phải nộp hồ sơ xin giấy phép nhập khẩu tại Bộ Y tế. Quy trình này bao gồm:
-
申請書を提出する: Hồ sơ được nộp qua cổng dịch vụ công trực tuyến của Bộ Y tế hoặc trực tiếp tại Vụ Trang thiết bị và Công trình y tế.
-
Thẩm định: Bộ Y tế sẽ kiểm tra hồ sơ, đánh giá tính hợp lệ và chất lượng của thiết bị.
-
Cấp phép: Nếu hồ sơ đạt yêu cầu, giấy phép nhập khẩu sẽ được cấp trong vòng 15-30 ngày làm việc.
注記: Một số thiết bị y tế đặc biệt (như thiết bị dùng trong nghiên cứu hoặc triển lãm) có thể được miễn giấy phép, nhưng cần xin xác nhận từ Bộ Y tế.
4. 通関手続きを行う
Sau khi có giấy phép, doanh nghiệp tiến hành nhập khẩu và thông quan hàng hóa tại cửa khẩu. Quy trình này bao gồm:
-
税関申告: Nộp tờ khai hải quan kèm các tài liệu như hóa đơn, 契約, 輸入ライセンス.
-
税金を支払う: Thiết bị y tế thường chịu thuế nhập khẩu và thuế giá trị gia tăng (バット). Một số thiết bị đặc biệt có thể được miễn giảm thuế theo quy định.
-
品質チェック: Hải quan có thể yêu cầu kiểm tra thực tế hàng hóa để đảm bảo phù hợp với hồ sơ đã nộp.
Doanh nghiệp nên làm việc với đơn vị logistics hoặc đại lý hải quan để đảm bảo quy trình thông quan diễn ra suôn sẻ.
5. 検査と回覧
通関後, thiết bị y tế cần được kiểm định chất lượng trước khi đưa vào lưu hành. Đối với thiết bị loại C, D, việc kiểm định phải được thực hiện bởi các tổ chức được Bộ Y tế chỉ định. Sau khi đạt yêu cầu, thiết bị sẽ được cấp số lưu hành để sử dụng hợp pháp tại Việt Nam.
6. 記録の保持とインポート後の追跡
Doanh nghiệp cần lưu trữ toàn bộ hồ sơ liên quan đến lô hàng trong thời gian tối thiểu 5 năm để phục vụ công tác kiểm tra, thanh tra. その上, cần theo dõi và báo cáo định kỳ về tình trạng sử dụng thiết bị y tế theo yêu cầu của cơ quan quản lý.
医療機器を輸入する際の注意事項
-
Chọn đối tác uy tín: Lựa chọn nhà cung cấp có uy tín, đảm bảo cung cấp đầy đủ giấy tờ hợp lệ và thiết bị đạt tiêu chuẩn.
-
Cập nhật quy định mới: Các quy định về nhập khẩu thiết bị y tế có thể thay đổi, vì vậy doanh nghiệp cần thường xuyên cập nhật thông tin từ Bộ Y tế hoặc các nguồn chính thống.
-
Hợp tác với đơn vị logistics chuyên nghiệp: Một đơn vị logistics có kinh nghiệm sẽ giúp xử lý các thủ tục hải quan và vận chuyển nhanh chóng, コスト削減.
-
Kiểm tra kỹ lô hàng: Trước khi nhập khẩu, cần kiểm tra kỹ thông tin lô hàng, đảm bảo không có sai sót về số lượng, chủng loại hoặc giấy tờ.
結論する
Nhập khẩu thiết bị y tế vào Việt Nam là một quá trình đòi hỏi sự chuẩn bị kỹ lưỡng và tuân thủ nghiêm ngặt các quy định pháp luật. Từ việc phân loại thiết bị, 記録を準備します, xin giấy phép đến thông quan và kiểm định, mỗi bước đều đóng vai trò quan trọng trong việc đảm bảo chất lượng và tính hợp pháp của thiết bị. Doanh nghiệp cần nắm rõ các quy định, phối hợp với các cơ quan chức năng và đối tác uy tín để thực hiện quy trình này một cách hiệu quả.
Với sự chuẩn bị chu đáo, việc nhập khẩu thiết bị y tế không chỉ đáp ứng nhu cầu thị trường mà còn góp phần nâng cao chất lượng chăm sóc sức khỏe tại Việt Nam.
クオン・コック・フレイト・フォワーディング・カンパニー・リミテッド
オフィス: 7階, パラマビル, 140バッハダン, タン・ソン・ホア・ワード, ホーチミン市
ホットライン: 0972 66 71 66
メール: info@cql.com.vn
Webサイト: https://cql.com.vn/

詳細をご覧ください