ヘルスケア業界が力強く成長する中で, 仕事 輸入 医療機器 増加する機器需要に対応するために、多くの企業にとって不可欠な活動になりつつあります。, 新しい技術. しかし, 輸入業務がスムーズに進むようにするため, 法律に従って, 企業は申請手続きが必要 輸入ライセンス 正確かつ完全に. 以下は、企業が適用に必要な手順を理解するのに役立つ詳細な手順です。 輸入ライセンス 2025年の医療機器.
記事の内容
2025年の医療機器輸入動向の概要
2025年, ヘルスケア業界は今後も拡大すると予想されています, 特に医療機器の輸入分野では, 検査・治療サービスの質の向上と新たな技術の導入の必要性から. 輸入医療機器はますます多様化, パラクリニカル機器から, 画像診断から複雑な治療支援装置まで. それが理由です, 法規制の遵守 医療機器を輸入する 法的リスクを回避し、持続可能な事業運営を確保するために非常に重要になります.

なぜ企業は通関前に輸入許可が必要なのでしょうか?
活動中 医療機器を輸入する, 輸入ライセンス 企業が市場に商品を持ち込むことを許可する州管理機関にとって、必須の法的証明書として機能します。. 具体的には, 輸入ライセンス ビジネスを助ける:
- 医療機器を輸入する前に保健省の法的要件を満たす.
- 有効なライセンスがないために罰金を科されたり、国境で商品が拘留されたりすることを避けてください。.
- 製品が品質基準を満たしていることを確認する, 規制に従って安全.
- 通関プロセスの最適化, 待ち時間を最小限に抑える.
ライセンスなしで輸入した場合の一般的な結果
意図的または非意図的な輸入 医療機器 でもまだ 輸入ライセンス 多くの深刻な結果を引き起こす可能性があります, 含む:
- 法律の規定に従って行政処分を受ける, 経済的損害や企業評判を引き起こす可能性がある.
- 商品は当局の規制に従って留置または廃棄されます.
- 事業計画の遅れ, 流通活動や顧客サービスに影響を与える.
- 重大な結果が生じた場合の刑事訴追のリスク.
申請プロセスを理解する 輸入ライセンス 企業がこれらのリスクを回避できるように支援する, 輸入業務の円滑化に貢献します, 法律上の.
これらの指示に完全に従うことで、企業がプロセスを明確に理解できるようになります。, 書類を期限内に完全に準備する, それにより、申請が成功する可能性が高まります 輸入ライセンス 2025年の医療機器.
2025年における医療機器輸入許可の最新法的根拠
医療業界の発展と革新が進む中、, 関連する法規制の更新 医療機器輸入許可 ビジネスが合法的かつ効果的に運営されるための重要な要素です. 2025年, これらの規制は、国際的な動向に準拠し、安全性を確保するために調整され続けています。, ユーザーにとっての品質. 以下は、今年の医療機器輸入活動に適用される最新の法的根拠の主な内容です。.

医療機器管理法: 政令 98/2021/ND-CP および政令 07/2023/ND-CP
現在の医療機器管理法は 2 つの重要な政令によって制度化されています。:
- 政令 98/2021/ND-CP: 管理規程, 分類する, 品質チェック, 医療機器の安全性と有効性, の条件を明確に定義します。 医療機器を輸入する 国内および国際規格に準拠している. この政令は、グループ A に応じた機器の分類に関する規定を更新しました。, B, C, D, 技術基準の拡充, 輸入許可手続き.
- 法令 07/2023/ND-CP: 継続と改訂, 違反の処理に関する追加コンテンツ, 検査工程, 医療機器を輸入する際の認証・許可手続き. この政令は、新たな規制を遵守する企業の責任も強調しています。, 輸入活動における法的リスクを最小限に抑える.
これら 2 つの法令は、運営の中核となる法的基盤です。 輸入ライセンス 医療機器, 企業が遵守しなければならない条件と手順を明確に規定する.
現在の案内状: 回覧 05/2022/TT-BYT および最新の更新
法令に加えて, 関連するガイダンス文書も、法執行機関を指導する上で重要な役割を果たします。:
- 回覧 05/2022/TT-BYT: プロセスに関する具体的な指示が記載された文書です, ファイル, 条件 医療機器輸入許可申請. この通達は、申請書の提出手順を規定しています。, チェック, 評価とライセンス, 技術基準と合わせて, 医療機器の安全性は最新の規制に準拠しています.
- この回覧の最新の更新には、出所を証明する文書への追加が含まれています, 領事合法化証明書, 高度医療機器の新たな技術基準, 検査規則も同様に, 認可後の監督.
これらの指示は、企業がプロセスを理解し、医療機器の輸入における法的規制を確実に遵守するのに役立ちます。, 法的リスクを回避し、違反に対処する.
輸入許可と医療機器流通番号の区別
法制度においては、 医療機器を輸入する, 2 つの重要な概念を明確に区別する必要があります:
- 輸入ライセンス: 企業が流通のために海外から医療機器をベトナムに持ち込むことを許可する国家管理機関が発行する証明書。, 特定の目的で配布または使用する. これは輸入活動を合法化するための必須条件です.
- 医療機器流通番号: デバイスのテスト後に発行される認証番号ですか, 技術的評価, 安全基準への準拠を確保する, 国内市場で流通および使用できる品質. 流通番号は、デバイスが正式に流通を承認されていることを示します。, 輸入ライセンスは流通チェーンの最初のステップにすぎません.
明確な区別により、企業は許可申請プロセス中の混乱を避けることができます。, 法的手続きの遵守を確保し、医療機器の輸入および流通に関連する法的リスクを回避します。. 同時に, これらの規制を理解することは、企業が文書を正確に識別するのにも役立ちます, 機器の種類ごとに輸入許可を申請するには書類を準備する必要があります.
それで, 2025 年も引き続き鮮明, 法的根拠の透明性 輸入ライセンス 医療機器, 経営効率の向上に貢献します, 地域の安全を確保し、現在の法規制に従って医療機器の輸入活動を促進する.
もっと参照してください: 通関サービス
医療機器の分類と輸入許可申請の条件
正しい医療機器グループを特定することは、申請プロセスにおける重要なステップです 輸入ライセンス 医療機器, 法的規制の遵守を確保し、望ましくない法的リスクを回避するため. 保健省の管理体制において, 医療機器は危険レベルに基づいて 4 つの主要なグループに分類されます。, 使用の性質とデバイスの複雑さ. 適切なグループを決定する方法は、企業が輸入手続きを実行するために必要な条件を理解するのに役立ちます.
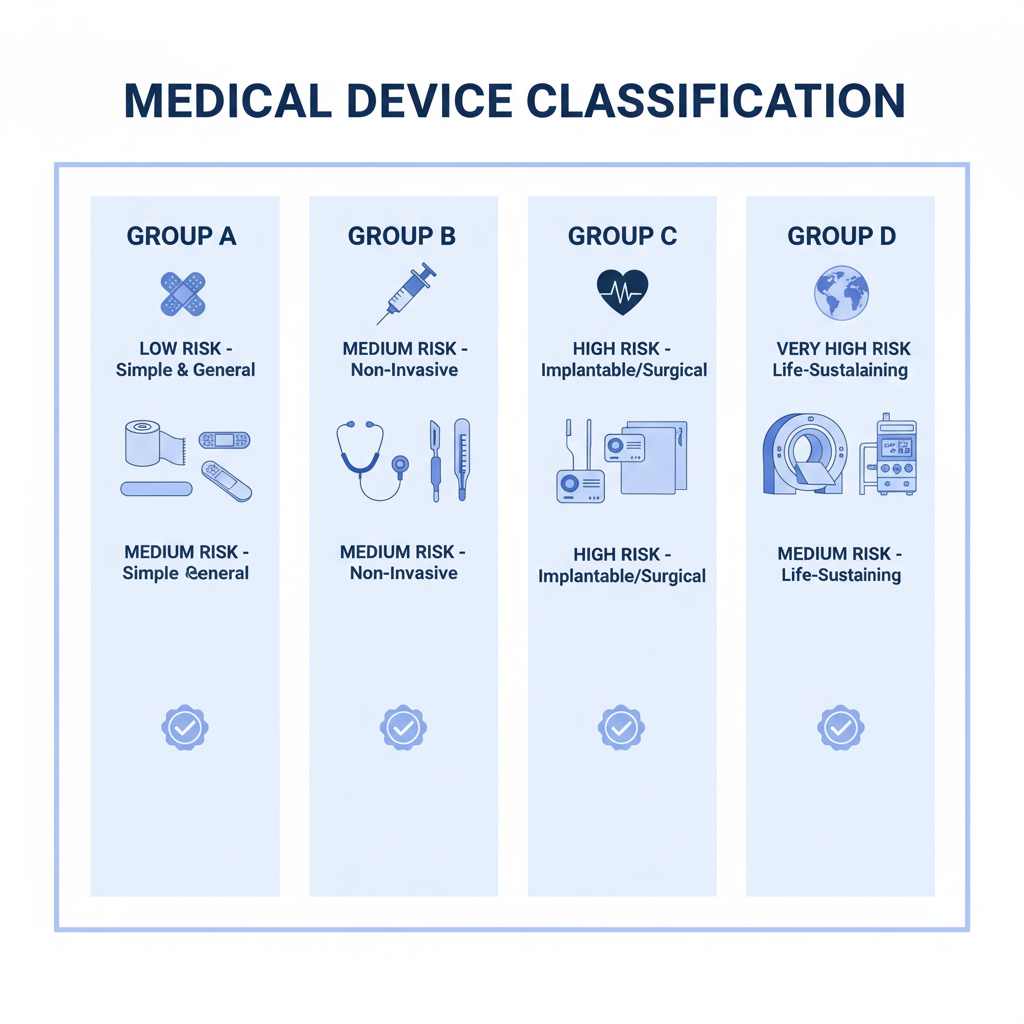
医療機器グループの識別方法 (グループA, B, C, D)
医療機器グループの決定は危険レベルの基準に基づいています, 特徴, そして使用目的. 具体的には, 決定する手順は次のとおりです:
- デバイスのプロパティを調査する: 仕様を見直す, メイン関数, およびデバイスアプリケーション.
- 危険度を考慮する: ユーザーの健康に害を及ぼす可能性や影響を与える可能性を評価する.
- 保健省の分類表を参照: 機器の分類に関する最新の規制を定期的に更新する.
- 適切なグループを特定する: 分析された基準に基づいて, グループAに属する機器を特定する, B, CまたはD.
これらのグループは次のように分類されます:
- グループA: 医療機器は危険性が低い, 通常は単純なデバイス, 非侵襲的、または身体への影響が少ない.
- グループB: 平均的な装備, 影響を与える可能性はありますが、ユーザーの健康に深刻な影響を与えることはありません.
- グループC: 設備にはより高いレベルの危険性があります, 侵襲性や重大な健康への影響と関連することが多い.
- グループD: 最も危険な装置, 多くの場合、複雑な機器が必要です, 適切に使用しないと潜在的に危険.
グループCのデバイス & Dは輸入ライセンスを申請する必要があります
現在の規制では, グループ C および D の機器が必要です 輸入ライセンス ベトナムで販売または使用される前に. この要件により、これらのデバイスが安全基準を満たしていることが保証されます, 品質と効率, および保健省の厳格な輸入管理規制に従っています。.
これらのデバイスには、次のようなタイプが含まれることがよくあります。:
- 複合画像診断装置 (MRI, CTスキャナ).
- ハイエンドの手術機器.
- 侵襲的または潜在的に危険な治療をサポートするデバイス.
- 臨床試験または研究で使用される医療機器.
これにより、管理機関は輸入医療機器の品質をより厳密に管理することができます。, 安全性と使用効率に関連するリスクを制限する.
医療機器の各グループの説明例
簡単に視覚化するために, 以下に各グループの例をいくつか示します。:
- グループA: 電子体温計などの機器, 自動血圧計, 針などの使い捨て医療機器, 包帯.
- グループB: 手持ち式超音波検査装置などの機器, 迅速試験機, シンプルな患者監視装置.
- グループC: デジタルレントゲン装置などの設備, 侵襲的機械換気装置, 内視鏡装置.
- グループD: MRI装置などの複合機器, CT装置, ロボット手術システム, 高精度の医療介入をサポートする機器.
正しい機器グループを特定することで、企業が手順を明確に定義できるようになります。, 準備が必要な書類と関連する法的条件, これにより、輸入プロセスがスムーズに進むようになります, より合法的かつより迅速に.
医療機器輸入許可申請の手順と書類
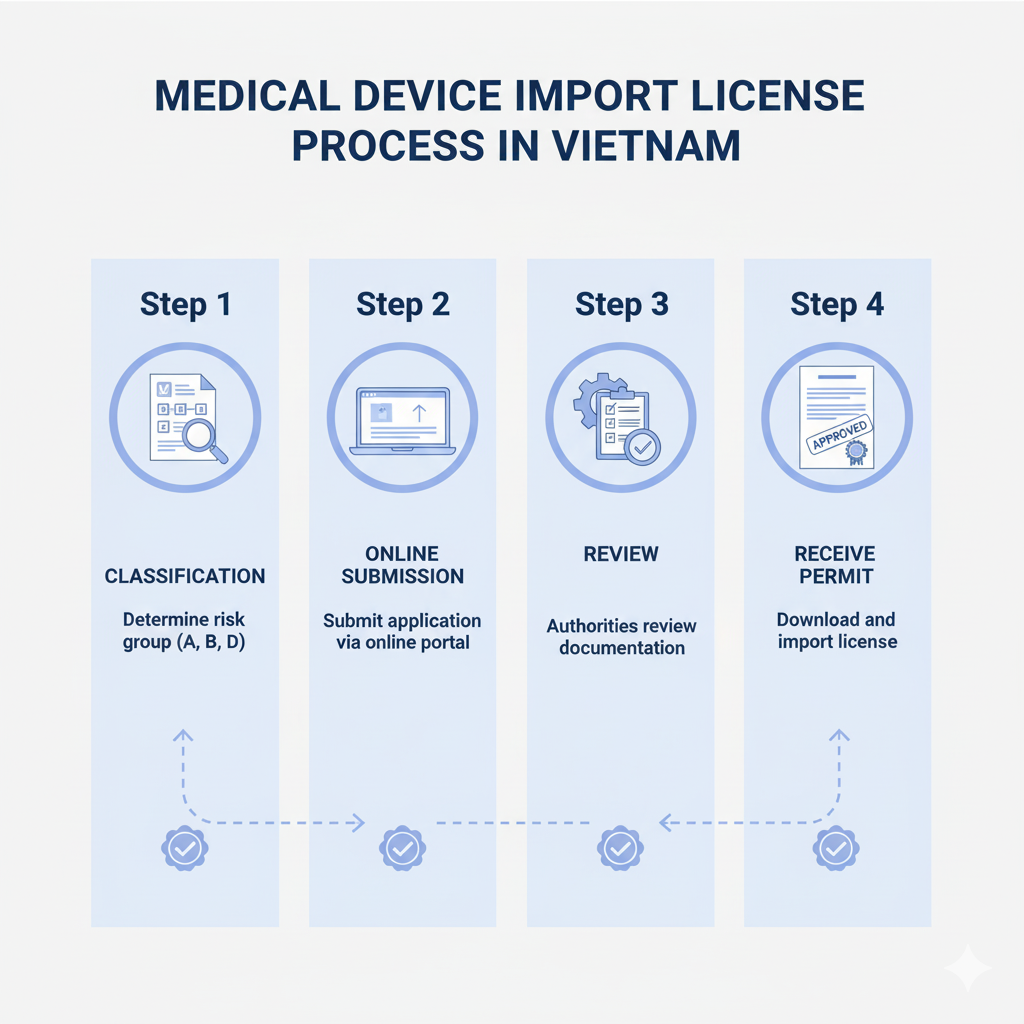
アプリケーション 輸入ライセンス 医療機器は、法律に従って輸入活動を行いたい企業にとって重要かつ必須のステップです。. このプロセスは、企業が商品の合法性を確保するだけでなく、法的リスクを回避するのにも役立ちます。, 罰金を科せられるか、国境ゲートでの通関を拒否される. 具体的な手続きの流れと申請に必要な書類は以下の通りです。 輸入ライセンス 2025年の最新規制に準拠した医療機器.
事業状況と輸入品 (CO, CQ, CFS, 自由流通証明書)
申請手続きを始める前に 輸入ライセンス, 企業は以下の条件を満たす必要があります:
- 企業は医療分野で事業を行うにはライセンスが必要です, 法律の規定に従って.
- 輸入製品は技術基準を満たしている必要があります, 規定に従った品質, 次のような法的起源を証明するすべての書類を用意してください。:
- 原産地証明書 (CO – 原産地証明書)
- 品質認証 (CQ – 資格証明書)
- 自由流通証明書 (CFS – 無料販売証明書)
- これらの文書は合法的である必要があります, それぞれの特定のタイプの医療機器に有効かつ適切です.
書類の準備が必要です: 申請フォーム, 権限, 技術文書, 有効な書類
申請手続きを行うため 輸入ライセンス, 企業は以下の種類の書類を十分に準備する必要があります:
- 輸入許可申請書 保健省発行のフォームによると.
- 委任状 企業から手続きを行う個人や団体まで.
- 医療機器の技術文書: カタログ付属, 使用説明書, 技術基準適合証明.
- 原産地を証明する有効な書類: CO, CQ, CFS, 自由流通証明書.
- 管轄当局が要求するその他の書類, 国際規格の証明書として (ISO, CE, FDA) ある場合.
注記, 外国の書類は、書類の有効性を確保するための規制に従って、ベトナムで領事館による合法化が必要です.
保健省公共サービスポータルを通じた申請プロセスと従うべき手順
申請の流れ 輸入ライセンス 保健省の公共サービスポータルを介した医療機器には、次の主な手順が含まれます:
- 記録を標準化する: ビジネスチェック, 書類をレビューする, 書類, 所定のリストに従って完全性と有効性を確保する.
- システムにログインする: 既存の登録アカウントを使用して保健省の公共サービス ポータルにアクセスします。.
- 情報を入力してプロフィールをダウンロード: 必要事項を記入し、用意した書類を添付してください.
- オンライン申請を提出する: システムを通じて書類を提出し、確認コードを受け取る.
- 処理の進行状況を監視する: プロファイルのステータスを更新する, 審査機関からの要求に応じて文書に回答または補足する.
- 結果を得る: 申請が承認されたとき, 企業は発行通知を受け取ります 輸入ライセンス システムまたはメール経由で.
- 印刷してアーカイブする: インポート作業で使用するライセンスを印刷します。, 規定に従って税関手続きを実施し、記録を保管する.
このプロセスを正しく実装すると、企業の処理時間の短縮に役立ちます, 医療機器輸入時の法令遵守の徹底とリスクの最小化.
時間, 輸入許可申請時の手数料と注意事項
申請手続き中 輸入ライセンス 医療機器用, 時間要因の理解, 料金と重要な注意事項は、企業がより積極的に計画を立て、発生するリスクを最小限に抑えるのに役立ちます。. ライセンスの手続きをスムーズに進めるために注意すべき内容は以下のとおりです, 効果的.
申請処理時間の制限と承認時間を短縮する方法
現在の規制によると, 輸入許可申請の処理時間 医療機器の場合、完全かつ有効な書類の受領日から平均 15 ~ 30 営業日かかります。. 書類に不足がある場合や追加の書類が必要な場合は、さらに時間がかかる場合があります, 書類. レビュー時間を短縮するには, 企業はすべきです:
- 完全な書類を準備する, 最初から合法かつ正確.
- 申請書を次の方法で提出してください 保健省公共サービスポータル 行政手続きの時間を最小限に抑えるため.
- システムを定期的に監視して、ライセンス発行機関からのフィードバックを更新します。.
- 緊急の必要がある場合, 企業はサポート サービスを利用して処理プロセスをスピードアップしたり、規制に従って特別な配慮を要求したりできます.
料金, サービスコストと手順を最適化する方法
関連料金 医療機器輸入許可申請 通常含まれている:
- 保健省の規定に基づく基本ライセンス料.
- 企業が手続きを行うためにコンサルティングサービスや代理店を雇う場合のサービス料.
- 検査に関わる手数料, 品質認証 (必要に応じて).
コストを最適化するには, 企業はできる:
- サービスコストを削減するために、保健省の指示に従って独自の書類を準備します。.
- 総合サービスを参照, 評判の良いユニットからの明確な時間とコストのコミットメントがある.
- エラーを最小限に抑えるために適切なサポート サービスを選択する, 申請をやり直す手間を省く, それによりコストと時間を節約します.
輸入ライセンスを申請する際の一般的なエラーとその修正方法
申請手続き中 輸入ライセンス, 企業では、次のような一般的なエラーが発生することがよくあります。:
- 間違った医療機器グループ: ライセンスの遅延または拒否を引き起こす. 保健省の分類に基づいて正しいデバイスグループを決定する必要があります.
- 書類が不足しているか無効です: 許可書などの書類の不備, 自由流通証明書 (CFS), 原産地証明書 (CO), 品質証明書 (CQ). それを修正するには, 申請書を提出する前に要件を注意深く確認し、十分な準備をする必要があります.
- 関係書類は規定に従って領事的に合法化されなかった: 書類検証で問題が発生する. 企業は、外国文書の有効性を確保するために、領事合法化プロセスに適切に従う必要があります。.
- プロフィールの情報が一致しません: 混乱や拒絶を引き起こす. 提出する前にデータを注意深く確認する必要があります.
これらのエラーの修正に注意すると、ライセンス プロセスがスムーズに進むようになります。, 時間とコストを節約します.
全体, 要因を理解する 時間, 料金 そして 重要な注意事項 申請手続き中に 輸入ライセンス 医療機器は企業が法規制を遵守するための重要な要素です, 期限の遅れや許可の拒否を避ける. 正しく練習しましょう, 完全な書類を準備する, 適切なサポートサービスを選択することで、輸入プロセスの効率向上とリスクの最小化に貢献します。.
許可が拒否された場合: 原因と治療法
申請手続き中 輸入ライセンス 医療機器, 企業の申請が拒否されるのは避けられない. この決定に至った理由を理解し、それに適切に対処する方法を知ることは、企業が残された問題を迅速に克服するのに役立ちます。, 時間を無駄にしないようにする, コストを削減し、法的規制を確実に遵守する. 以下は、この状況が発生した場合の一般的な原因と解決策の詳細な分析です。.
輸入許可の拒否につながる一般的な原因
ライセンス付与の拒否は、多くの場合、次の主な理由から発生します。:
- 記録の欠落またはエラー: 申請フォーム 輸入ライセンス 不完全または不正確な情報が最も一般的な原因です. これには、自由流通証明書などの必要書類の不足も含まれます。 (CFS), 原産地証明書 (CO), 品質証明書 (CQ), または技術的な記録が不明瞭である.
- 医療機器の分類に適合しない: 企業が規制に従って医療機器グループを正しく識別していない, 不適切な文書、または各グループの特定の要件を満たさない文書が作成される.
- 医療機器は輸入対象外: 機器が技術基準を満たしていない, 十分な有効な証明書を持っていない, または、法律に基づく有効な自由流通証明書を持っていない.
- 法的文書または領事認証における誤り: 海外からの書類は無効です, 正しい手続きに従って領事的に合法化されていない, または出所に関する書類が不足している, 品質.
- 申請手続きに従わない場合: 公共サービスポータルを通じて書類を誤って提出した場合, チェック手順が不足している、または必要に応じて最新のレコードを更新できない.
改訂の指示, 書類を補足して免許を再申請する
拒否されたとき, 企業は修正を行うには次の手順を実行する必要があります, 書類を補充して再申請する 輸入ライセンス 効果的に:
- 拒否の正確な原因を特定する: ライセンス機関の決定をよく読み、その理由を明確に理解してください。. 通常, 代理店は記録に不備や矛盾がある場合は明確に通知します。.
- 追加書類を準備する, 適当な編集: フィードバック内容をもとに, 企業は不足している文書または無効な文書を更新または補足する必要がある, 領事合法化証明書として, 技術基準適合証明, または製品の原産地に関する文書.
- 必要な編集を行う: すべての書類が正しいことを確認してください, クリア, 政令 98/2021/ND-CP の規定に従って完全かつ有効, 回覧 05/2022/TT-BYT および最新の指示.
- 公共サービスポータルから修正書類を提出する: 編集完了後, 企業は保健省の電子システム経由で申請書を提出する必要がある, 手順が正しく実行されていることを確認してください.
- 進捗状況を確認するには直接連絡してください: サポートが必要な場合や質問がある場合は、, 企業は申請処理担当者に直接連絡してプロセスを理解し、迅速なフィードバックを受け取ることができます。.
ライセンスを再申請する必要がある場合とその手順
いくつかの特殊な場合, 申請が拒否されるか、ライセンスが取り消される, 企業は再申請を余儀なくされる 輸入ライセンス 最初から. 手順は次のとおりです:
- 取り消しまたは拒否の理由を明確に特定する: 所属事務所の発表をよく読んで正確な原因を知りましょう, そこから適切な治療法が生まれます.
- 編集, 新しいプロフィールを完成させる: すべての書類を保護する, 認証, 必要に応じて適切かつ有効な書類, 追加の新しい書類や国際規格への準拠証明書が必要になる場合があります.
- もう一度申請書を提出してください: 公共サービスポータルを通じて、または管轄当局に直接申請プロセスに従ってください。.
- 承認を待ち、進捗状況を監視する: このプロセス中に, 企業は文書のステータスを定期的に確認する必要がある, ライセンス機関からの要求に応じて、コンテンツを追加または明確にする準備ができています.
- 新しいライセンスを取得する 申請が正常に承認され、完全な法的条件が保証された後.
ライセンス拒否に対する迅速かつ正確な処理により、企業は時間を節約できます, 法的リスクを回避する, 同時に、医療機器の合法的かつ効果的な輸入を維持します。.
[h2] CUONG QUOC Logistics社の医療機器輸入許可申請サポートサービス
[h3] 充実したサービスのご紹介, CONG QUOC物流の専門的な作業プロセス
ますます厳格化する法的背景と医療機器の輸入に対する高い要件, CUONG QUOC Logisticsは自信を持ってサポートサービスを提供します 輸入ライセンス 専門的な医療機器, パッケージ, 企業が複雑な法的手続きを実行する際の時間と労力を最大限に節約できるように支援します.
私たちは、医療機器の輸入時に法的規制を遵守することの重要性を理解しています。, 同時に、明確なプロセスによるサービスの提供にも努めます。, 透明, 機器分類ステップから, 提出用の書類を準備し、結果を追跡する. CUONG QUOC Logisticsの作業プロセスには主な手順が含まれます:
- 要請を受けて輸入が必要な医療機器の種類を分析する
- 条件など詳しくご相談させていただきます, 書類を準備する必要がある
- 企業が規制に従って完全かつ有効な文書を作成できるようにサポートします。
- 保健省の公共サービスポータルを通じて申請を提出してください
- モニター, レビュープロセスを更新し、編集リクエストに迅速に対応します
- 輸入ライセンスを受け取り、企業を次のステップに導きます
私たちは医療分野の多くの企業の信頼できるパートナーであることを誇りに思っています, 経験豊富な専門家のチームを所有しています, 常に最新の規制を正確に更新します 輸入ライセンス 医療機器.
[h3] 時間の約束, 費用や手続きの無料相談など
CUONG QUOC Logisticsはお客様にサービスを提供することに尽力しています。:
- 処理時間が速い, 予定通りに確実に行う, 企業による医療機器の早期稼働を支援します
- リーズナブルなコスト, クリア, サービスのパフォーマンス中に隠れたコストが発生することはありません
- 無料相談, 企業が法的規制を理解できるようにサポートする, 必要な条件, 申請手続きの準備が必要 輸入ライセンス 順調に進みました, スムーズに
その上, 書類の合法性チェックなどの付随サービスも提供します, 拒否されたレコードの編集手順, 企業が申請手続きの成功について絶対的な安心感を得るのに役立ちます 輸入ライセンス 医療機器.
私たちはそれを理解しています, それぞれの顧客には独自のニーズと特性があります, したがって、CUONG QUOC Logisticsのサービスは常に柔軟です, 各ビジネスの要件に応じてカスタマイズ. 当社のコンサルティングチームはいつでも耳を傾けます, 分析, 最適なソリューションを提供します, 顧客の時間を節約するのに役立ちます, 医療機器輸入の際のコストを削減し、法的リスクを最小限に抑えます。.
顧客満足をモットーに, CUONG QUOC Logistics は、申請プロセス全体を通じてビジネスに同行することに尽力します。 輸入ライセンス, すぐに結果が得られます, 2025 年の現在の法規制に正確に準拠.
結論する
医療業界はますます発展し、高品質が求められるようになってきています。, 医療機器の輸入に関連する法規制の遵守は、事業運営を円滑かつ合法的に行うための重要な要素となります。. この記事では、2025年の医療機器輸入動向について詳しく説明しています。, 通関前の輸入許可の重要性を強調した, 正しい手順に従わない場合に発生する可能性のある重大な結果だけでなく、.
Decree 98/2021/ND-CP などの最新の法規制, 法令 07/2023/ND-CP および通達 05/2022/TT-BYT などの指導通達は、企業が機器グループを決定する際の強固な法的基盤を提供します。, 許可申請および必要な書類の準備に関する条件.
その上, この記事では、申請プロセスの手順もわかりやすく説明しています。, 処理時間, 料金の準備が必要です, 一般的なエラーと、ライセンスが拒否された場合の問題の対処方法について説明します。. 特別, CUONG QUOC Logistics のサポート サービスは企業の時間節約に役立ちます, 医療機器の輸入許可申請のプロセスにおけるコストを削減し、リスクを最小限に抑える.

詳細をご覧ください