在医疗保健行业强劲增长的背景下, 工作 进口 医疗设备 成为许多企业不可或缺的活动,以满足日益增长的设备需求, 新技术. 然而, 确保进口业务顺利进行, 依法, 企业需办理申请手续 进口许可证 准确、完整. 以下是详细说明,可帮助企业了解申请的必要步骤 进口许可证 2025年医疗设备.
文章内容
2025年医疗器械进口趋势概览
2025年, 预计医疗保健行业将持续扩张, 尤其是在进口医疗器械领域, 由于需要提高医疗检查和治疗服务质量以及应用新技术. 进口医疗器械日益多元化, 来自辅助临床设备, 诊断成像到复杂的治疗支持设备. 这就是为什么, 遵守法律规定 进口医疗设备 对于避免法律风险以及确保可持续的业务运营变得极其重要.

为什么企业在清关前需要进口许可证?
活动中 进口医疗设备, 进口许可证 作为国家管理机构允许企业将商品带入市场的强制性法律证书。. 具体来说, 进口许可证 帮助企业:
- 进口医疗设备前符合卫生部的法律要求.
- 避免因缺乏有效许可证而被罚款或货物在边境被扣留.
- 确保产品符合质量标准, 按规定安全.
- 优化清关流程, 最大限度地减少等待时间.
无证进口的常见后果
有意或无意的进口 医疗设备 但还没有 进口许可证 可能会导致许多严重的后果, 包括:
- 依法给予行政处分, 可能造成财务损失和企业声誉.
- 根据当局规定扣留或销毁货物.
- 推迟商业计划, 影响分销活动和客户服务.
- 造成严重后果的可能面临刑事起诉.
了解申请流程 进口许可证 帮助企业规避这些风险, 有助于确保进口活动顺利进行, 合法的.
完全遵循这些说明将有助于企业清楚地了解该流程, 充分、准时准备文件, 从而提高申请成功的可能性 进口许可证 2025年医疗设备.
2025年医疗器械进口许可证最新法律依据
在医疗行业日益发展和创新的背景下, 更新相关法律法规 医疗器械进口许可证 是企业合法有效经营的关键因素. 2025年, 这些规定不断调整,以顺应国际趋势并确保安全, 用户质量. 以下是今年适用于医疗器械进口活动的最新法律依据的主要内容。.

医疗器械管理法: 第 98/2021/ND-CP 号法令和 07/2023/ND-CP 号法令
现行医疗器械管理法通过两项重要法令制度化:
- 第 98/2021/ND-CP 号法令: 管理规定, 分类, 质量检查, 医疗设备的安全性和有效性, 其中明确规定了条件 进口医疗设备 符合国家和国际标准. 本法令更新了按照 A 组对设备进行分类的规定, 乙, C, D, 扩大技术标准, 和进口许可程序.
- 07/2023/ND-CP 号法令: 延续和修订, 与处理违规行为相关的附加内容, 检验流程, 进口医疗设备的认证和许可程序. 该法令还强调了企业遵守新法规的责任, 最大限度降低进口活动的法律风险.
这两条法令是运营的核心法律基础 进口许可证 医疗设备, 明确规定企业必须遵守的条件和程序.
目前的指导通告: 通告 05/2022/TT-BYT 和最新更新
除了法令之外, 相关指导性文件也对执法具有重要指导作用:
- 通告 05/2022/TT-BYT: 是包含流程具体说明的文档, 文件, 条件 申请进口医疗器械许可证. 本通知规定了提交申请的步骤, 查看, 评估和许可, 以及技术标准, 医疗设备安全符合最新法规.
- 本通告的最新更新包括对原产地证明文件的补充, 领事认证证书, 高端医疗器械新技术标准, 以及检验规定, 许可后监管.
这些说明可帮助企业了解医疗设备进口的流程并确保遵守法律法规。, 规避法律风险,处理违规行为.
进口许可证与医疗器械流通编号的区别
在法律体系中关于 进口医疗设备, 有必要明确区分两个重要概念:
- 进口许可证: 由国家管理机构颁发的证书,允许企业将医疗设备从国外带入越南流通。, 出于特定目的分发或使用. 这是进口活动合法化的强制性条件.
- 医疗器械流通编号: 设备测试后是否颁发认证号码, 技术评估, 确保符合安全标准, 国内市场分销和使用的质量. 流通编号表明该器械已正式批准流通, 进口许可证只是分销链的第一步.
明确区分有助于企业避免在许可证申请过程中出现混乱, 确保遵守合法程序,避免医疗设备进口和分销相关的法律风险. 同时地, 了解这些规定也有助于企业准确识别文件, 申请适合每种设备的进口许可证需要准备文件.
所以, 2025 年形势继续明朗, 法律依据透明 进口许可证 医疗设备, 有助于提高管理效率, 根据现行法律规定确保社区安全并促进医疗设备进口活动.
查看更多: 报关服务
医疗器械分类及申请进口许可证条件
识别正确的医疗器械组是申请过程中的重要一步 进口许可证 医疗设备, 确保遵守法律法规并避免不必要的法律风险. 在卫生部的管理体系中, 医疗器械根据危险级别分为四大类, 设备的使用性质和复杂性. 如何确定合适的群体有助于企业了解办理进口手续的必要条件.
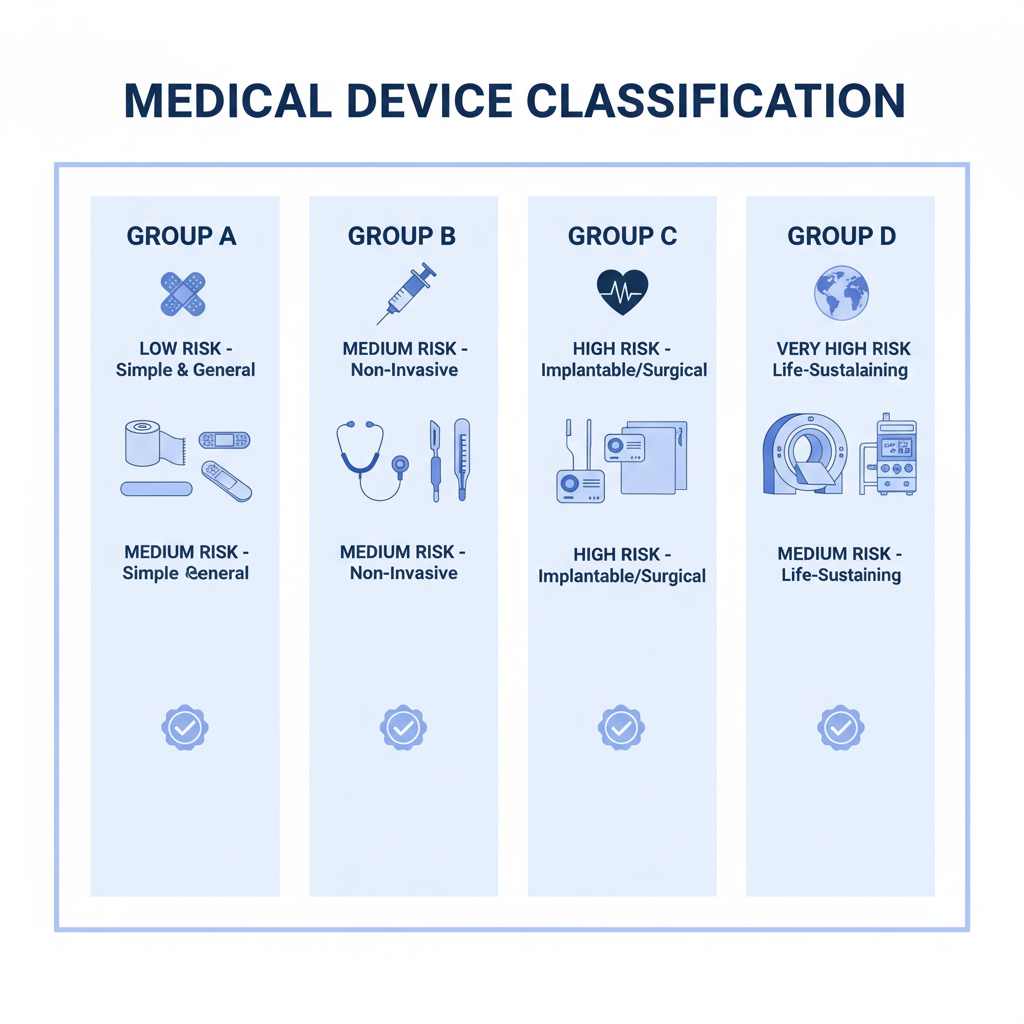
如何识别医疗器械类别 (A组, 乙, C, D)
医疗器械类别的确定以危险级别为标准, 特征, 和预期用途. 具体来说, 确定步骤如下:
- 研究设备的属性: 查看规格, 主要功能, 和设备应用.
- 考虑危险程度: 评估造成伤害或影响用户健康的可能性.
- 参见卫生部分类清单: 定期更新设备分类最新规定.
- 确定正确的群体: 基于分析的标准, 识别属于 A 组的设备, 乙, 绳索.
这些组分类如下:
- A组: 医疗器械危险性较小, 通常是简单的设备, 无创或对身体影响很小.
- B组: 装备一般, 有可能造成影响,但不会严重影响用户的健康.
- C组: 设备危险等级较高, 通常与侵入性或重大健康影响有关.
- D组: 最危险的装置, 往往涉及复杂的设备, 如果使用不当可能存在危险.
C组设备 & D 需申请进口许可证
在现行规定中, 需要 C 组和 D 组的设备 进口许可证 在投放市场或在越南使用之前. 此要求确保这些设备符合安全标准, 质量和效率, 以及符合卫生部严格的进口管制规定.
这些设备通常包括以下类型::
- 复杂影像诊断设备 (核磁共振成像, CT扫描仪).
- 高端手术设备.
- 支持侵入性或潜在危险治疗的设备.
- 用于临床试验或研究的医疗器械.
这有助于管理机构更严格地控制进口医疗设备的质量, 限制与使用安全和效率相关的风险.
每组医疗器械的说明性示例
为了方便可视化, 以下是每个组的一些说明性示例:
- A组: 电子体温计等设备, 自动血压计, 一次性医疗器械,例如针头, 绷带.
- B组: 手持式超声机等设备, 快速测试机, 简单的病人监护设备.
- C组: 数字X光机等设备, 有创机械通气设备, 内窥镜装置.
- D组: MRI 机等复杂设备, CT机, 机器人手术系统, 支持高精度医疗干预的设备.
识别正确的设备组有助于企业明确定义程序, 需要准备的文件及相关法律条件, 从而保证进口过程的顺利进行, 更合法、更快捷.
申请进口医疗器械许可证的程序及文件
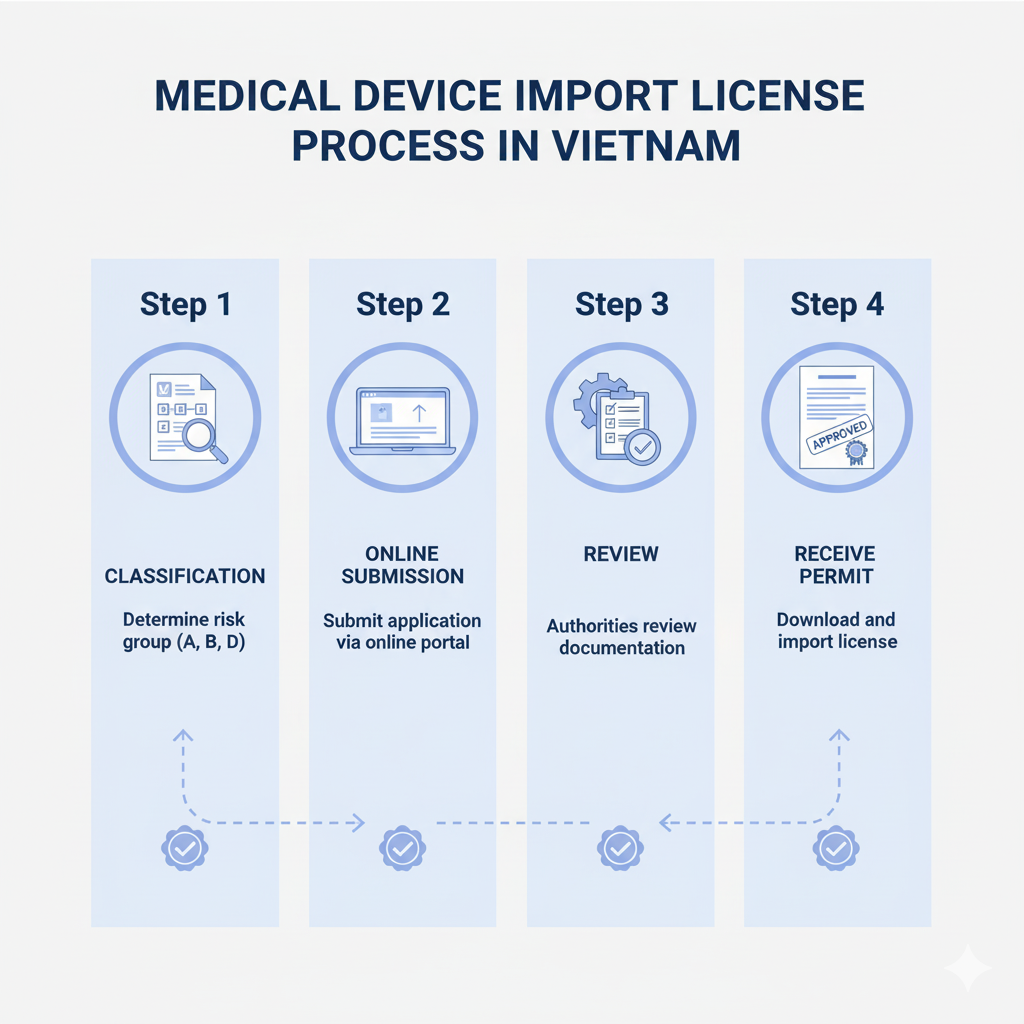
应用 进口许可证 对于想要依法开展进口活动的企业来说,医疗设备是重要且强制性的一步。. 这一流程不仅可以帮助企业确保其商品的合法性,还可以避免法律风险, 被罚款或被拒绝在边境口岸通关. 以下是申请的具体步骤以及需要准备的文件 进口许可证 符合2025年最新法规的医疗设备.
企业及进口产品情况 (一氧化碳, 重庆, 慢性疲劳综合症, 自由流通证书)
开始申请程序之前 进口许可证, 企业需满足以下条件:
- 企业必须拥有医疗领域经营许可证, 依照法律规定.
- 进口产品必须符合技术标准, 质量符合规定, 拥有所有证明合法来源的文件,例如:
- 原产地证书 (CO——原产地证书)
- 质量认证 (CQ-- 资格证书)
- 自由流通证书 (CFS – 自由销售证书)
- 这些文件必须是合法的, 有效且适合每种特定类型的医疗器械.
需要准备文件: 申请表, 权威, 技术文件, 有效证件
办理申请手续 进口许可证, 企业需充分准备以下几类文件:
- 进口许可证申请表 根据卫生部发出的表格.
- 授权书 从企业到执行程序的个人或组织.
- 医疗器械技术文件: 包括目录, 使用说明, 符合技术标准的认证.
- 证明原产地的有效文件: 一氧化碳, 重庆, 慢性疲劳综合症, 自由流通证书.
- 主管机关要求的其他文件, 作为国际标准的证书 (国际标准化组织, CE, 美国FDA) 如果有的话.
笔记, 外国文件需按规定在越南进行领事认证,以确保文件的有效性.
通过卫生部公共服务门户网站的申请流程和遵循的步骤
申请流程 进口许可证 通过卫生部公共服务门户获取医疗设备包括以下主要步骤:
- 标准化记录: 商业支票, 审查文件, 文档, 根据规定清单确保完整性和有效性.
- 登录系统: 使用您现有的注册帐户访问卫生部公共服务门户.
- 填写信息并下载简介: 填写所有必要的信息并附上准备好的文件.
- 提交在线申请: 通过系统提交文件并收到确认码.
- 监控处理进度: 更新个人资料状态, 应审查机构要求回复或补充文件.
- 获取结果: 申请获批准时, 企业将收到发行通知 进口许可证 通过系统或通过电子邮件.
- 打印并存档: 打印用于进口活动的许可证, 按规定办理海关手续并储存记录.
正确实施此流程有助于企业缩短处理时间, 确保医疗设备进口过程中的合法合规性并最大程度地降低风险.
时间, 申请进口许可证的费用及注意事项
申请过程中 进口许可证 用于医疗设备, 对时间因素的理解, 费用以及重要说明将帮助企业更加主动地进行规划并最大程度地减少产生的风险. 为了顺利办理牌照,需要注意以下内容, 有效的.
申请处理时限以及如何缩短审批时间
根据现行规定, 进口许可证申请的处理时间 医疗设备从收到完整有效的文件之日起平均需要15至30个工作日. 如果文件丢失或需要额外文件,这个时间可能会更长, 文档. 以缩短审稿时间, 企业应该:
- 准备完整的文件, 从一开始就合法准确.
- 通过以下方式提交您的申请 卫生部公共服务门户 尽量减少行政程序时间.
- 定期监控系统以更新许可机构的反馈.
- 如果有紧急需要, 企业可以聘请支持服务来加快处理流程或根据规定要求特殊考虑.
费用, 服务成本以及如何优化流程
相关费用 申请进口医疗器械许可证 通常包括:
- 基本许可费按卫生部规定执行.
- 如果企业聘请咨询服务或代理来办理手续,则需支付服务费.
- 检验相关费用, 质量认证 (如果需要的话).
优化成本, 企业可以:
- 根据卫生部的指示自行准备文件,以降低服务成本.
- 参考综合服务, 有信誉单位明确的时间和成本承诺.
- 选择正确的支持服务以最大限度地减少错误, 避免重做您的申请, 从而节省成本和时间.
申请进口许可证时的常见错误及其解决方法
申请过程中 进口许可证, 企业经常会遇到一些常见错误,例如::
- 错误的医疗器械组: 导致许可延迟或被拒绝. 需要根据卫生部的分类确定正确的器械组.
- 文件缺失或无效: 缺乏授权等文件, 自由流通证书 (慢性疲劳综合症), 原产地证书 (一氧化碳), 质量证书 (重庆). 修复它, 提交申请前您需要仔细查看要求并做好充分准备.
- 档案未按规定办理领事认证: 导致文件验证出现问题. 企业应妥善办理领事认证流程,确保涉外文书的有效性.
- 个人资料上的信息不匹配: 造成混乱或拒绝. 提交前需仔细核对数据.
注意修复这些错误将有助于许可过程顺利进行, 节省时间和成本.
全面的, 了解因素 时间, 费用 和 重要提示 申请过程中 进口许可证 医疗设备是企业确保合法合规的关键因素, 避免逾期或拒绝许可证. 正确练习, 准备完整的文件, 选择合适的支持服务将有助于提高进口过程中的效率并最大限度地降低风险.
当许可被拒绝时: 原因及治疗
申请过程中 进口许可证 医疗设备, 企业的申请被拒绝是不可避免的. 了解导致这一决定的原因并了解如何适当处理将有助于企业快速克服剩余的问题。, 避免浪费时间, 成本并确保遵守法律法规. 下面详细分析常见原因以及遇到这种情况时的解决方法.
导致进口许可证被拒绝的常见原因
拒绝颁发许可证往往来自以下主要原因:
- 记录缺失或错误: 申请表 进口许可证 信息不完整或不准确是最常见的原因. 这包括缺乏必要的文件,例如自由流通证书 (慢性疲劳综合症), 原产地证书 (一氧化碳), 质量证书 (重庆), 或技术记录不清楚.
- 不符合医疗器械分类: 企业未按规定正确识别医疗器械类别, 导致文件不适合或不符合各组的具体要求.
- 医疗设备不符合进口资格: 设备不符合技术标准, 没有足够的有效认证, 或不具备依法自由流通的有效凭证.
- 法律文件或领事认证错误: 国外的文件无效, 未按照正确程序进行领事认证, 或缺乏与原产地相关的文件, 质量.
- 不遵守申请程序: 通过公共服务门户错误提交文件, 缺乏检查步骤或未按要求更新最新记录.
修改说明, 补充文件并重新申请许可证
被拒绝时, 企业需采取以下步骤进行修改, 补充材料并重新申请 进口许可证 有效地:
- 确定拒绝的确切原因: 仔细阅读许可机构的决定,清楚了解原因. 通常情况下, 该机构将明确通知您记录中的任何缺陷或差异.
- 准备额外文件, 适当的编辑: 根据反馈内容, 企业需要更新或补充缺失或无效的文件, 作为领事认证证书, 符合技术标准的认证, 或与产品原产地相关的文件.
- 进行必要的编辑: 确保所有文件均正确, 清除, 根据第 98/2021/ND-CP 号法令的规定,完整且有效, 通告 05/2022/TT-BYT 和最新说明.
- 通过公共服务门户提交修改后的文件: 完成编辑后, 企业需要通过卫生部的电子系统提交申请, 确保正确执行步骤.
- 直接联系以监控进度: 如果您需要支持或有疑问, 企业可以直接联系申请处理官员,了解流程并获得快速反馈.
如果您需要重新申请许可证以及采取的步骤
在一些特殊情况下, 申请被拒绝或执照被吊销, 企业被迫重新申请 进口许可证 从一开始. 步骤如下:
- 明确撤销或拒绝的原因: 仔细阅读管理机构的公告,了解具体原因, 从那里,会有适当的治疗方法.
- 编辑, 完成新的个人资料: 保护所有文件, 认证, 根据需要提供适当且有效的文件, 可能需要额外的新文件或符合国际标准的证明.
- 再次提交您的申请: 通过公共服务门户网站或直接在主管部门办理申请流程.
- 等待批准并监控进度: 在此过程中, 企业需要定期检查其文件的状态, 如果许可机构要求,准备提供额外或澄清的内容.
- 获取新许可证 申请成功获批并具备充分的法律条件后.
快速正确地处理许可证拒绝问题将帮助企业节省时间, 规避法律风险, 同时,保持医疗器械进口合法有效.
[小时2] CUONG QUOC Logistics 申请医疗设备进口许可证的支持服务
[小时3] 推出综合服务, CONG QUOC Logistics专业的工作流程
在日益严格的法律环境和对医疗器械进口的高要求下, CUONG QUOC Logistics 很荣幸能够提供支持服务 进口许可证 专业医疗设备, 包裹, 帮助企业最大限度地节省执行复杂法律程序的时间和精力.
我们了解医疗设备进口过程中遵守法律法规的重要性, 同时,我们致力于提供流程清晰的服务, 透明的, 从设备分类步骤, 准备提交文件并跟踪结果. CUONG QUOC Logistics 的工作流程包括主要步骤:
- 接收请求并分析需要进口的医疗设备类型
- 详细条件咨询, 需要准备文件
- 支持企业按规定准备完整有效的文件
- 通过卫生部公共服务门户提交申请
- 监视器, 更新审阅流程并快速响应编辑请求
- 获得进口许可证并指导企业进行后续步骤
我们很荣幸成为医疗领域众多企业值得信赖的合作伙伴, 拥有一支经验丰富的专业团队, 时刻准确更新最新法规 进口许可证 医疗设备.
[小时3] 时间承诺, 费用和免费咨询程序
CUONG QUOC Logistics 致力于为客户提供:
- 快速处理时间, 确保按计划进行, 帮助企业医疗设备尽快投入运营
- 成本合理, 清除, 服务执行过程中不会产生隐性成本
- 免费咨询, 支持企业了解法律法规, 必要条件, 申请过程中需要准备的程序 进口许可证 进展顺利, 顺利
除了, 我们还提供检查文件合法性等伴随服务, 编辑拒绝记录的说明, 帮助企业对申请程序的成功感到绝对放心 进口许可证 医疗设备.
我们明白, 每个客户都有自己的需求和特点, 因此,CUONG QUOC Logistics 的服务始终是灵活的, 根据每个企业的需求进行个性化定制. 我们的咨询团队随时准备倾听, 分析, 提供最优化的解决方案, 帮助客户节省时间, 降低医疗设备进口过程中的成本和法律风险.
以客户满意为中心的座右铭, CUONG QUOC Logistics 致力于在整个申请过程中陪伴企业 进口许可证, 提供快速结果, 2025年完全符合现行法律规定.
结论
在医疗保健行业日益发展和高品质要求的背景下, 遵守进口医疗设备的相关法律法规成为确保业务顺利合法开展的关键因素。. 文章详述了2025年进口医疗设备的趋势, 强调清关前进口许可证的重要性, 以及如果不遵循正确的程序可能发生的严重后果.
最新法律法规,如第 98/2021/ND-CP 号法令, 第 07/2023/ND-CP 号法令和第 05/2022/TT-BYT 号通知等指导性通知为企业确定设备组提供了坚实的法律基础。, 申请许可的条件和准备完整的文件.
除了, 文章还清楚地指导了申请过程的步骤, 处理时间, 需要准备费用, 以及常见错误以及许可被拒绝时如何处理问题. 特别的, CUONG QUOC Logistics 的支持服务帮助企业节省时间, 医疗器械进口许可证申请过程中的成本和风险最小化.

查看更多